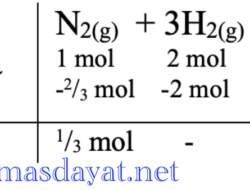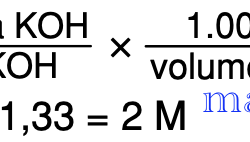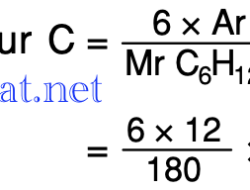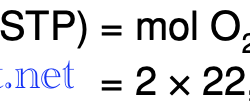kali ini kita akan membahas soal berikut nya… Perhatikan persamaan reaksi berikut! N2(g) + H2(g) → NH3(g) Jika 1 mol N2 direaksikan dengan […]
MaztaH
Sebanyak 5,4 gram aluminium dilarutkan dalam 400 mL tembaga (II) sulfat 0,5 M menurut persamaan
kali ini kita akan membahas soal berikut nya… Sebanyak 5,4 gram aluminium dilarutkan dalam 400 mL tembaga (II) sulfat 0,5 […]
Diketahui 6,4 gram metana dibakar dengan 16 gram gas oksigen menurut reaksi berikut.
kali ini kita akan membahas soal berikut nya… Diketahui 6,4 gram metana dibakar dengan 16 gram gas oksigen menurut reaksi […]
Setarakan persamaan reaksi berikut! a. N2(g) + H2(g) → NH3(g) b. Ca(OH)2(aq) + H3PO4(aq)
kali ini kita akan membahas soal berikut nya… Setarakan persamaan reaksi berikut! a. N2(g) + H2(g) → NH3(g) b. Ca(OH)2(aq) + H3PO4(aq) → Ca3(PO4)2(aq) + H2O(l) c. NaOH(aq) + […]
Sebanyak 84 gram KOH (Mr = 56) dilarutkan dalam 750 mL air. Tentukan konsentrasi larutan tersebut!
kali ini kita akan membahas soal berikut nya… Sebanyak 84 gram KOH (Mr = 56) dilarutkan dalam 750 mL air. […]
Diketahui massa atom relatif (Ar) dari H = 1, C = 12, O = 16. Tentukan persentase massa unsur C dalam
kali ini kita akan membahas soal berikut nya… Diketahui massa atom relatif (Ar) dari H = 1, C = 12, […]
Hitunglah banyaknya molekul senyawa yang terdapat dalam 2 mol Na2SO4
kali ini kita akan membahas soal berikut nya… Hitunglah banyaknya molekul senyawa yang terdapat dalam 2 mol Na2SO4! Jawab: N […]
Hitunglah banyaknya molekul senyawa yang terdapat dalam 2 mol Na2SO4
kali ini kita akan membahas soal berikut nya… Hitunglah banyaknya molekul senyawa yang terdapat dalam 2 mol Na2SO4! Jawab: N […]
Jika tetapan Avogadro = L, tentukan banyaknya atom nitrogen yang terkandung dalam 1 gram gas
kali ini kita akan membahas soal berikut nya… Jika tetapan Avogadro = L, tentukan banyaknya atom nitrogen yang terkandung dalam […]
Tentukan volume dari 2 mol O2 pada kondisi STP
kali ini kita akan membahas soal berikut nya… Tentukan volume dari 2 mol O2 pada kondisi STP! Jawab: Pada kondisi STP […]